Bệnh hemoglobin niệu kịch phát ban đêm (PNH)
1 PNH là gì
2 Triệu chứng
3 Chẩn đoán
4 Diễn biến lâm sàng
5 Điều trị
6 Tiên lượng
7 Mong muốn có con/mang thai
8 Đăng ký
1 PNH là gì
1.1 Tổng quan
Giống như thiếu máu bất sản, hemoglobin niệu kịch phát ban đêm (PNH) không phải là bệnh ác tính, nhưng là bệnh rất hiếm gặp và có thể đe dọa tính mạng. Bệnh này do một khiếm khuyết di truyền mắc phải của các tế bào gốc tạo máu trong tủy xương, không phải là bệnh di truyền.
1.2 Tỷ lệ mắc bệnh (dịch tễ học)
Tỷ lệ mắc bệnh (tỷ lệ mắc) là 1-2 ca mới trên 1 triệu người mỗi năm. Tuy nhiên, do các triệu chứng rất đa dạng, có thể giả định rằng PNH hiếm khi được chẩn đoán hoặc chỉ được chẩn đoán muộn, vì bệnh này thường không được phát hiện ngay lập tức. Bệnh thường được chẩn đoán nhất ở độ tuổi từ 25 đến 45, với tỷ lệ mắc bệnh ở nam và nữ gần như bằng nhau. Không có sự tập trung gia đình.
1.3 Nguồn gốc (bệnh sinh)
PNH xảy ra do một sự thay đổi di truyền (đột biến) của các tế bào gốc tạo máu trong tủy xương. Sự thay đổi này không có từ khi sinh ra, mà chỉ xuất hiện trong quá trình sống (đột biến gen somatic) và không thể di truyền cho con cái. Các tế bào khỏe mạnh và tế bào bệnh cùng tồn tại song song (mosaic).
Đột biến gen này thường nằm trong một đoạn đặc biệt của gen, gen PIG-A, và ảnh hưởng đến một hoặc nhiều tế bào gốc tạo máu trong tủy xương. Gen này tạo ra một chất xúc tác sinh học (enzyme), thường được sử dụng để sản xuất một hệ thống neo đặc biệt, neo glycosylphosphatidylinositol (neo GPI). Neo này nằm trên màng tế bào và có chức năng gắn kết nhiều protein trên màng tế bào, trong đó có chức năng điều hòa hệ miễn dịch. Bằng cách này, chúng bảo vệ các tế bào khỏi sự tấn công của một phần nhất định của hệ miễn dịch, được gọi là hệ thống bổ sung, bằng cách đánh dấu các tế bào là “không phải ngoại lai”.
Hai trong số các protein này đóng vai trò đặc biệt quan trọng:
- Yếu tố tăng tốc phân hủy bổ sung (DAF, CD55)
- Protectin (MAC-IP: Protein ức chế phức hợp tấn công màng, MIRL: Chất ức chế phân hủy phản ứng màng, CD59)
Sự giảm hoặc thiếu hụt hoàn toàn các protein gắn GPI trên màng tế bào hồng cầu, bạch cầu và tiểu cầu làm cho các tế bào này dễ bị phá hủy bởi hệ thống bổ sung. Điều này dẫn đến sự vỡ hồng cầu PNH trong mạch máu (huyết tán nội mạch) và kích hoạt tiểu cầu (PNH), có thể dẫn đến huyết khối.
Hệ thống bổ sung giúp cơ thể chống lại các tác nhân gây nhiễm trùng, ký sinh trùng, các phân tử lạ, v.v. Khi hệ thống này được kích hoạt, một quá trình liên tiếp như thác nước (thác bổ sung) sẽ bắt đầu, có thể dẫn đến sự phá hủy tế bào mục tiêu.
2 Triệu chứng
Các triệu chứng và triệu chứng của PNH có thể khác nhau và xuất hiện tạm thời hoặc liên tục. Ngoài ra, khi hệ thống bổ sung được kích hoạt do nhiễm trùng, mang thai hoặc căng thẳng, các triệu chứng có thể trở nên trầm trọng hơn, dẫn đến sự phân hủy mạnh mẽ của các tế bào hồng cầu (khủng hoảng tan máu). Trong quá trình điều trị bằng chất ức chế bổ sung, hiện tượng này còn được gọi là tan máu đột phá. Một dấu hiệu cảnh báo điển hình và rõ ràng cho tình trạng này là nước tiểu có màu sẫm hoặc đen (hemoglobin niệu). Nguy cơ huyết khối cũng tăng cao trong trường hợp này.
Trong những giai đoạn này, thường cần phải truyền máu (huyết cầu đỏ cô đặc, EK) hoặc các liệu pháp điều trị khác.
Nếu PNH không được điều trị, tình trạng này có thể đe dọa tính mạng.
2.1 Giảm số lượng tế bào (cytopenia)
Thiếu máu (anemia)
Sự phân hủy các tế bào hồng cầu (tan máu) có thể dẫn đến thiếu máu (anemia) và do đó thiếu chất vận chuyển oxy (hemoglobin).
Các triệu chứng bao gồm:
- Da nhợt nhạt (dấu hiệu không đặc hiệu)
- Suy giảm sức khỏe, khó tập trung, trầm cảm, mệt mỏi, chân nặng, nhanh mệt
- Khó thở (khó thở) khi gắng sức do số lượng chất vận chuyển oxy giảm
- Chóng mặt, ù tai, nhịp tim nhanh (nhịp tim nhanh), đau ngực (đau thắt ngực), rối loạn thị giác
Tình trạng thiếu máu có thể nghiêm trọng đến mức cần phải truyền hồng cầu (huyết sắc tố cô đặc).
Các dòng tế bào khác bị giảm
Ngoài dòng tế bào hồng cầu, các dòng tế bào máu khác cũng có thể bị giảm (cytopenia), ví dụ như tiểu cầu (thrombocytopenia) hoặc bạch cầu hạt (neutropenia). Điều này thường là biểu hiện của bệnh thiếu máu bất sản kèm theo.
2.2 Tác động của tan máu
Khi hồng cầu bị phân hủy, sự phân hủy hemoglobin làm tăng lượng bilirubin trong máu. Điều này có thể dẫn đến da và phần trắng bên ngoài của nhãn cầu (sklera). Tình trạng này được gọi là vàng da (ikterus hoặc sklerenikterus).
Ngoài ra, khi các tế bào hồng cầu bị phân hủy, hemoglobin sẽ được giải phóng. Khi lượng hemoglobin tự do tăng cao, nó có thể được bài tiết qua thận và dẫn đến nước tiểu có màu sẫm, nâu đỏ hoặc thậm chí đen (hemoglobinuria).
Qua các bước phân hủy khác nhau, hemoglobin tự do dẫn đến giảm sự sẵn có của oxit nitric (NO). Oxit nitric cần thiết cho sự giãn nở của cơ trơn, ví dụ như trong đường tiêu hóa, mạch máu hoặc phổi. Nếu không có đủ oxit nitric, cơ trơn sẽ căng thẳng, dẫn đến co thắt, co mạch máu và tăng huyết áp.
Cơ chế hoạt động này giải thích nhiều triệu chứng lâm sàng của PNH:
- Đau bụng dữ dội, thường là đau cấp tính
- Co thắt thực quản kèm theo khó nuốt (khó nuốt)
- Huyết áp cao
- Áp lực cao trong tuần hoàn phổi (tăng áp động mạch phổi) kèm theo khó thở
- Suy giảm chức năng thận
- Rối loạn cương dương (rối loạn chức năng cương dương)
2.3 Mệt mỏi (Fatigue)
Mệt mỏi là tình trạng mệt mỏi hoặc kiệt sức kéo dài bất thường, có thể ảnh hưởng đáng kể đến khả năng hoạt động thể chất và tinh thần. Đặc điểm của mệt mỏi là tình trạng này không cải thiện hoặc chỉ cải thiện không đáng kể ngay cả khi nghỉ ngơi hoặc ngủ nhiều hơn.
Một nguyên nhân có thể gây ra mệt mỏi liên quan đến PNH là thiếu hụt oxit nitric (NO) do thiếu máu và sự phá hủy các tế bào hồng cầu. Tuy nhiên, mệt mỏi cũng có thể do các rối loạn khác của hệ thống miễn dịch hoặc chuyển hóa.
2.4 Xu hướng huyết khối (thrombophilia)
Một trong những hậu quả nguy hiểm nhất của PNH không được điều trị và sự thiếu hụt oxit nitric (NO) do đó là sự hình thành cục máu đông (huyết khối). Sự thiếu hụt này kích hoạt các tiểu cầu, dẫn đến sự hình thành cục máu đông một cách bất thường. Các cục máu đông này có thể làm tắc nghẽn các mạch máu nhỏ và dẫn đến nhồi máu ở các cơ quan bị ảnh hưởng. Nhiều bộ phận khác nhau của cơ thể có thể bị ảnh hưởng, ví dụ như gan hoặc não, cả các mạch máu dẫn máu về (tĩnh mạch) và các mạch máu cung cấp máu (động mạch). Tương tự, sự tích tụ cao của hemoglobin tự do có thể dẫn đến suy thận cấp tính.
3 Chẩn đoán
Phương pháp kiểm tra ưa thích để chẩn đoán PNH là phương pháp đo lưu lượng tế bào. Phương pháp này rất nhạy cảm và do đó có thể phát hiện một số lượng rất nhỏ các tế bào bị biến đổi bệnh lý. Ngoài ra, tỷ lệ tế bào bị ảnh hưởng (kích thước klon PNH) và các loại tế bào bị ảnh hưởng, ví dụ như hồng cầu, bạch cầu hạt hoặc bạch cầu đơn nhân, có thể được xác định rất chính xác. Để thực hiện xét nghiệm này, máu được lấy từ tĩnh mạch (máu ngoại vi).
Khi chẩn đoán lần đầu, cần thực hiện thêm các xét nghiệm khác:
- Tiền sử bệnh (tiền sử bệnh), bao gồm cả tiền sử gia đình, bao gồm các câu hỏi cụ thể về các triệu chứng điển hình của PNH, xem 2 Triệu chứng
- Khám sức khỏe, chú ý các khía cạnh đặc biệt nêu trên: dấu hiệu thiếu máu, vàng da (ikterus), dấu hiệu huyết khối cấp tính hoặc trước đó, dấu hiệu chảy máu, bất thường về thể chất như trong trường hợp thiếu máu bất sản bẩm sinh (xem ở đó), lá lách to (splenomegalia)
- Kiểm tra tế bào
-
- Hình ảnh vi thể tế bào máu khác biệt
- Kiểm tra tế bào hồng cầu non, chưa trưởng thành trong máu (hồng cầu lưới)
-
- Hóa học lâm sàng
-
- Các thông số tan máu: đặc biệt là LDH, haptoglobin, bilirubin
- Các thông số chức năng thận: creatinine, bão hòa transferrin
- Mức vitamin B12 và axit folic
- Tình trạng sắt: Ferritin, transferrin, bão hòa transferrin, hemoglobin reticulocyte. Với giá trị ferritin > 1000-2000 µg/l, tùy theo diễn biến, cần tiến hành kiểm tra các tổn thương cơ quan có thể xảy ra do quá tải sắt.
- Giá trị BNP trong huyết thanh để đánh giá chức năng của tâm thất phải như một dấu hiệu của tăng áp động mạch phổi (tăng huyết áp phổi)
-
- Chẩn đoán chức năng
- Siêu âm vùng bụng (abdomen)
- Siêu âm tim
- Chức năng phổi
- Điện tâm đồ (EKG)
Chẩn đoán tủy xương bằng mô học, cytology, cytogenetics và molecular genetics nên được thực hiện tại thời điểm chẩn đoán ban đầu. Điều này đặc biệt quan trọng khi đồng thời có cytopenia ở mức độ cao đến mức nghi ngờ PNH có liên quan đến một bệnh huyết học khác, ví dụ như thiếu máu bất sản hoặc hội chứng myelodysplastic (MDS).
Khi phát hiện tế bào PNH (clone PNH) hoặc chẩn đoán hội chứng suy tủy xương (Bone Marrow Failure Syndrome, BMFS), cần tiến hành kiểm tra, đặc biệt là trong hai năm đầu tiên sau chẩn đoán ban đầu, cứ 6 tháng một lần và khi có các triệu chứng mới xuất hiện. Tỷ lệ tương đối của PNH-Klon (kích thước PNH-Klon) trong tổng số tế bào tủy xương có thể dao động và rất quan trọng đối với diễn biến tiếp theo của bệnh cũng như việc xác định và kiểm soát liệu pháp điều trị.
4 Diễn biến lâm sàng
4.1 Tổng quan
Các triệu chứng và vấn đề của PNH có thể rất khác nhau và dẫn đến suy giảm chất lượng cuộc sống do các triệu chứng nêu trên.
Các cơ chế của bệnh được mô tả có thể dẫn đến tăng huyết áp, tăng áp lực trong tuần hoàn phổi (tăng áp động mạch phổi) và rối loạn chức năng thận. Những thay đổi này có thể dẫn đến tổn thương vĩnh viễn và cần được theo dõi liên tục.
4.2 Cục máu đông (huyết khối/thromboembolism)
Biến chứng nghiêm trọng nhất của PNH là sự hình thành cục máu đông (thrombosis/thromboembolism), dẫn đến tắc nghẽn mạch máu. Theo các nghiên cứu, xác suất xảy ra thrombosis là
– 30% trong vòng 10 năm nếu không có liệu pháp điều trị cụ thể (chất ức chế bổ sung, ức chế kết tập tiểu cầu)
– 30-50% trong quá trình bệnh nếu không có biện pháp điều trị cụ thể
Các biến chứng huyết khối tắc mạch là nguyên nhân gây ra tới 67% tổng số ca tử vong do PNH. Ngay cả những bệnh nhân PNH chỉ có một số ít tế bào PNH cũng có nguy cơ huyết khối cao. Khả năng bị huyết khối có thể phụ thuộc vào kích thước của dòng tế bào PNH.
Huyết khối ở bệnh nhân PNH xuất hiện ở những vị trí điển hình và ít điển hình hơn:
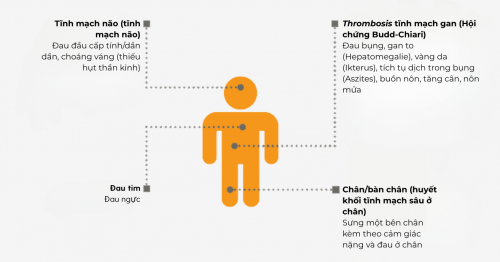
Huyết khối ở bệnh nhân PNH xuất hiện ở những vị trí điển hình và ít điển hình hơn.
4.3 Rối loạn chức năng thận
Hai phần ba số bệnh nhân PNH bị suy giảm chức năng thận. Chức năng lọc bị suy giảm là nguyên nhân chính dẫn đến sự suy giảm khả năng lọc máu của thận. Chỉ số được sử dụng để đánh giá chức năng thận là độ thanh thải creatinine, cho biết thời gian cần thiết để lọc creatinine, một sản phẩm phân hủy của cơ, khỏi huyết tương. Cả chức năng lọc và độ thanh thải creatinine đều có thể suy giảm trong quá trình tiến triển của bệnh.
4.4 Giảm số lượng tế bào (cytopenia)
Sự giảm rõ rệt số lượng tế bào máu do bệnh tủy xương kèm theo là nguyên nhân thứ hai gây ra các biến chứng nghiêm trọng, chiếm 20% các trường hợp. Khoảng 15% bệnh nhân phát triển thiếu máu bất sản với sự thiếu hụt cả ba dòng tế bào máu (pancytopenia). Ngược lại, thiếu máu bất sản cũng có thể xuất hiện trước, sau đó PNH mới xuất hiện.
5 Điều trị
5.1 Tổng quan
Việc điều trị PNH phụ thuộc vào mức độ nghiêm trọng của các triệu chứng và biểu hiện. Nếu không có triệu chứng đáng kể, chỉ cần theo dõi chặt chẽ là đủ. Có thể xem xét các biện pháp hỗ trợ và sử dụng thuốc ức chế đông máu (chống đông máu), thường được gọi là thuốc làm loãng máu. Chống đông máu không thực sự làm loãng máu, mà ngăn ngừa sự tắc nghẽn (“đặc”) của mạch máu do cục máu đông. Trong trường hợp PNH có triệu chứng, hình thức điều trị phụ thuộc vào mức độ nghiêm trọng của sự phá hủy hồng cầu (tan máu) và sự hiện diện của huyết khối hoặc cục máu đông.
Biểu đồ sau đây trình bày phương pháp điều trị PNH tan máu:
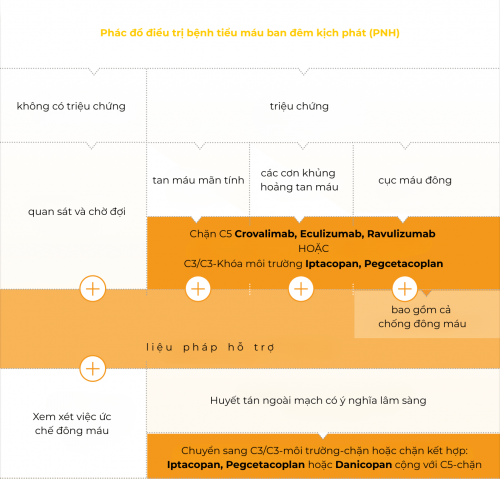
Biểu diễn đơn giản hóa của thuật toán điều trị. Thuật toán đầy đủ được trình bày trong hướng dẫn của DGHO trên Onkopedia.
5.2 Điều trị cụ thể
Vì hệ thống bổ sung Vì hệ thống bổ sung (xem 4.1.3) tấn công các tế bào hồng cầu PNH bị biến đổi bệnh lý, thuốc được sử dụng ở đây. Chúng được gọi là chất ức chế bổ sung và ức chế một phần của hệ thống bổ sung. Do đó, chúng ức chế hoặc ngăn chặn hoàn toàn sự phá hủy các tế bào hồng cầu. Mục tiêu của liệu pháp sử dụng chất ức chế bổ sung là tránh các biến chứng nghiêm trọng, đe dọa tính mạng và các tổn thương có thể xảy ra.
Các lý do y tế để điều trị bằng Eculizumab/Ravulizumab bao gồm
- Cục máu đông
- Đau bụng cấp tính
- Các cơn tan máu
- Rối loạn chức năng thận do PNH
- Cần truyền máu
- Tăng áp lực động mạch phổi (tăng huyết áp phổi) liên quan đến PNH
Ức chế bổ sung C5
Các liệu pháp điều trị PNH có mục tiêu được phê duyệt lâu nhất là kháng thể chống C5 Eculizumab (Soliris®) được giới thiệu vào năm 2007 và dạng tác dụng dài Ravulizumab (Ultomiris®) được phê duyệt vào năm 2019.
Hai hoạt chất này ngăn chặn hoạt động của protein C5 trong hệ thống bổ sung (được gọi là ức chế bổ sung cuối cùng). Các nghiên cứu khác nhau đã chỉ ra rằng Eculizumab và Ravulizumab làm giảm đáng kể sự phá hủy trực tiếp các tế bào hồng cầu trong mạch máu (huyết tán nội mạch) nhờ sự ngăn chặn này.
Kết quả là chất lượng cuộc sống của các bệnh nhân PNH được điều trị bằng Eculizumab/Ravulizumab được cải thiện đáng kể. Điều này thậm chí còn được quan sát thấy ở những bệnh nhân không có sự bình thường hóa nồng độ hemoglobin. Điều này cho thấy rằng ngoài việc cải thiện tình trạng thiếu máu, một phần tác dụng của thuốc là do ngăn chặn sự phá hủy hồng cầu (huyết tán).
Liệu pháp đặc hiệu này đã làm giảm đáng kể nhu cầu truyền máu, thiếu máu, mệt mỏi (mệt mỏi), đau bụng cấp tính, cũng như giảm huyết áp cao (tăng huyết áp động mạch) và huyết áp cao ở phổi (tăng huyết áp phổi). Ngoài ra, các nghiên cứu còn mô tả sự cải thiện hoặc thậm chí bình thường hóa chức năng thận sau khi có thể đã bị rối loạn chức năng thận trước đó.
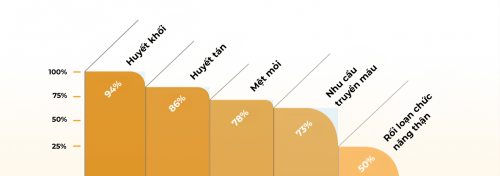
Tác dụng của Eculizumab trong điều trị PNH
Eculizumab hoặc Ravulizumab được tiêm vào tĩnh mạch (tiêm tĩnh mạch) và có thể được thực hiện tại phòng khám ngoại trú. Thông thường, Eculizumab được tiêm truyền một lần mỗi tuần trong 4 tuần đầu tiên để đạt nồng độ tối đa, sau đó tiêm truyền 2 tuần một lần để duy trì liều lượng. Ngược lại, Ravulizumab phải được tiêm truyền 2 lần trong vòng 2 tuần để đạt nồng độ tối đa, sau đó chỉ tiêm truyền 8 tuần một lần để duy trì liều lượng. Khác với Eculizumab, liều lượng Ravulizumab phụ thuộc vào trọng lượng cơ thể. Thời gian truyền tĩnh mạch lại phụ thuộc vào liều lượng.
Với Crovalimab (Piasky®), từ năm 2024, một loại kháng thể Anti-C5 khác đã có sẵn, có thể được tiêm dưới da (tiêm dưới da) với liều lượng nhỏ hơn sau khi tiêm tĩnh mạch (truyền) một lần. Trong trường hợp này, cần phải điều trị duy trì 4 tuần một lần.
Trong khi sự phá hủy các tế bào hồng cầu trong mạch máu (tan máu nội mạch) được ức chế thành công bằng ức chế bổ sung cuối cùng với Eculizumab/Ravulizumab/ Crovalimab, một phần bệnh nhân hiện nay lại bị suy giảm chậm các hồng cầu bị biến đổi bệnh lý bên ngoài mạch máu (tan máu ngoài mạch máu). Quá trình này được kích hoạt bởi sự tích tụ các tiền chất của hệ thống bổ sung và có thể được phát hiện bằng các xét nghiệm máu đặc biệt (bao gồm reticulocytes, giá trị bilirubin, xét nghiệm Coombs). Ức chế sự phá hủy các tế bào hồng cầu bên ngoài mạch máu là điểm khởi đầu cho việc phát triển các loại thuốc mới.
Ức chế bổ sung C3
C3-inhibitor (inhibitor bổ sung gần) ức chế bổ sung trong chuỗi phản ứng sớm hơn C5-inhibitor. Do đó, có thể giảm hoặc ngăn chặn sự nạp các tiền chất bổ sung vào các tế bào PNH và do đó giảm hoặc ngăn chặn sự tan máu ngoài mạch máu. Các chất mới này bao gồm C3-inhibitor Pegcetacoplan, yếu tố D Danicopan và chất ức chế yếu tố B Iptacopan. Giống như toàn bộ hệ thống bổ sung, các yếu tố B và D cũng là các protein.
(Hình minh họa sẽ được cung cấp sau)
Pegcetacoplan (Aspaveli®) phải được tiêm dưới da (tiêm dưới da) 2-3 lần/tuần trong khoảng 1 giờ.
Danicopan (Voydeya®) dưới dạng thuốc viên phải được dùng thêm 150-200 mg 3 lần/ngày bên cạnh liệu pháp điều trị bằng Eculizumab hoặc Ravulizumab.
Iptacopan (Fabhalta®) được dùng dưới dạng thuốc viên (viên nang) với liều 200 mg 2 lần/ngày như một liệu pháp đơn trị.
Nhìn chung, dữ liệu từ các nghiên cứu phê duyệt và các đánh giá hiện tại về liệu pháp dài hạn cho thấy đây là các liệu pháp hoặc thuốc rất dễ dung nạp. Một tác dụng phụ rất phổ biến là đau đầu, chỉ xảy ra ở giai đoạn đầu của liệu pháp. Các tác dụng phụ khác có thể xảy ra bao gồm nhiễm trùng, thay đổi công thức máu, mất ngủ, rối loạn tiêu hóa, vấn đề về da, các triệu chứng giống cúm và mệt mỏi.
Ngoài ra, một điều đáng chú ý là các bệnh nhân PNH phàn nàn nhiều hơn về đau đầu sau khi dùng thuốc ức chế bổ sung lần đầu tiên. Triệu chứng này là dấu hiệu cho thấy thuốc có hiệu quả tốt. Do số lượng hồng cầu bị phân hủy ít hơn, nên lượng oxit nitric (NO) có sẵn lại nhiều hơn. Do đó, các mạch máu có thể giãn nở, nhưng cơ thể phải làm quen lại với trạng thái bình thường này.
Do sự phân hủy của các tế bào hồng cầu bị bệnh giảm, lượng hemoglobin và do đó lượng sắt được bài tiết qua nước tiểu cũng giảm hoặc không còn nữa. Với việc loại bỏ sự mất sắt mãn tính qua thận, một số bệnh nhân PNH được điều trị có sự gia tăng lượng sắt dự trữ. Do đó, lượng sắt dự trữ cần được kiểm tra thường xuyên, đặc biệt là khi kèm theo thiếu máu bất sản, để có thể ngừng điều trị bằng viên sắt kịp thời (mục tiêu ferritin > 100 µg/l) và nếu cần thiết, loại bỏ lượng sắt dư thừa bằng liệu pháp chelat.
Tuy nhiên, liệu pháp ức chế bổ sung không làm giảm số lượng tế bào bệnh hoặc chữa khỏi bệnh. Ngược lại, nhờ sự bảo vệ của ức chế bổ sung, ít hoặc không có tế bào hồng cầu bị biến đổi bệnh lý bị phân hủy, do đó số lượng tế bào hồng cầu tăng lên. Sự gia tăng của các hồng cầu PNH hoặc giá trị hemoglobin là dấu hiệu cho thấy hiệu quả của liệu pháp. Do đó, việc điều trị thường xuyên hoặc uống thuốc thường xuyên là rất quan trọng để đảm bảo bảo vệ liên tục các tế bào bị bệnh và tránh các biến chứng của PNH (tan máu đột ngột) đã đề cập.
Tiêm phòng
Tiêm phòng là cần thiết vì cơ thể không thể bảo vệ mình đủ trước các vi khuẩn có vỏ bọc (meningococcus, pneumococcus và haemophilus influenzae) do hệ thống bổ sung bị ức chế. Các vi khuẩn này có thể gây ra nhiễm trùng nghiêm trọng, ví dụ như nhiễm trùng máu, viêm phổi, viêm màng não do vi khuẩn. Do đó, khi điều trị bằng Eculizumab/Ravulizumab/Crovalimab, việc tiêm phòng ngừa vi khuẩn não mô cầu là bắt buộc. Cần phải sử dụng hai loại vắc-xin khác nhau (Menveo®/Nimenrix® và Bexsero®/Trumenba®) để bao phủ càng nhiều chủng vi khuẩn não mô cầu càng tốt (A, C, W135, Y khi bắt đầu điều trị và B trong quá trình điều trị), mặc dù vậy vẫn không thể đạt được sự bảo vệ 100%. Cần tiêm vắc-xin phòng ngừa mỗi ba năm một lần.
Ngoài ra, bệnh nhân được điều trị bằng Pegcetacoplan hoặc Iptacopan còn phải tiêm vắc-xin phòng ngừa vi khuẩn phế cầu (Prevenar 20®) và Haemophilus influenzae loại B (ActHib® hoặc Hiberix®). Vắc-xin phòng ngừa vi khuẩn phế cầu nên được tiêm lại sau mỗi 6 năm. Vaccine phòng ngừa Haemophilus chỉ tiêm một lần.
Mặc dù đã tiêm vaccine, các bệnh nhiễm trùng nghiêm trọng kèm theo nhiễm trùng máu (sốc nhiễm trùng) vẫn có thể xảy ra, do đó, luôn tuân thủ các quy tắc hành vi sau:
Khi bị sốt (nhiệt độ > 38,3 °C), phát ban, cảm giác ốm nặng, cứng cổ, nhiễm trùng đường hô hấp nặng, điều quan trọng là phải tiến hành “điều trị dự phòng” (ví dụ: Amoxicillin/Clavulanic acid 1000 mg) càng sớm càng tốt và đến gặp bác sĩ ngay lập tức để tiến hành chẩn đoán thêm và nếu cần thiết, bắt đầu điều trị kháng sinh mở rộng.
Ngoài ra, cần thảo luận với bác sĩ huyết học điều trị về tình trạng tiêm chủng hiện tại, đặc biệt là về các loại vắc-xin tiêm bổ sung như cúm, COVID-19, virus hợp bào hô hấp (RSV), zona (herpes zoster) và vắc-xin tiêm nhắc lại.
5.3 Điều trị triệu chứng
Ngoài các chất ức chế bổ sung đã nêu, còn có các phương pháp khác để điều trị các triệu chứng chung.
Trong trường hợp có triệu chứng thiếu máu, có thể tiêm huyết cầu đỏ. Mặc dù truyền máu sẽ cung cấp một lượng nhỏ các yếu tố bổ sung, nhưng điều này sẽ không làm tăng quá trình tan máu do bổ sung. Điều này cũng áp dụng cho việc sử dụng huyết tương tập trung, xem Thiếu máu bất sản, 5.5 Điều trị hỗ trợ > Truyền máu.
Nếu PNH không liên quan trực tiếp đến suy tủy xương, nó được gọi là “PNH cổ điển”. Nếu không được điều trị, tình trạng thiếu sắt thường xảy ra do mất hemoglobin liên tục qua thận. Vì sắt cần thiết cho quá trình hình thành hồng cầu, nên trong những trường hợp này, bệnh nhân phải được bổ sung sắt. Sắt có thể được bổ sung dưới dạng viên nén hoặc truyền tĩnh mạch. Tốt nhất, thuốc uống nên được dùng vào buổi sáng mỗi hai ngày một lần khi bụng đói. Ngoài ra, không nên dùng sắt cùng với thuốc kháng sinh hoặc thuốc trung hòa axit dạ dày (thuốc kháng axit). Khi bắt đầu điều trị bằng sắt, cần kiểm tra thường xuyên quyết định điều trị bổ sung sắt. Để làm điều này, cần kiểm tra nồng độ ferritin trong các cuộc kiểm tra y tế (mục tiêu ferritin > 100 µg/l).
Do sự bù đắp tăng cường tái tạo hồng cầu, nhu cầu axit folic và vitamin B12 cũng tăng lên. Trong trường hợp này, nên bổ sung 5 mg axit folic mỗi ngày hoặc 1-2 lần/tuần. Nếu thiếu vitamin B12, nên bổ sung trong một thời gian nhất định.
Trong các nghiên cứu trước đây, người ta đã quan sát thấy rằng nguy cơ huyết khối có liên quan đến số lượng tế bào PNH và mức độ hoạt động tan máu. Nếu tỷ lệ bạch cầu hạt bị rối loạn GPI cao hơn 50% và/hoặc giá trị LDH cao hơn 1,5 lần so với giá trị bình thường, thì nguy cơ huyết khối sẽ tăng lên đáng kể. Khi những bệnh nhân này được dùng thuốc chống đông máu phòng ngừa, họ ít bị huyết khối hơn đáng kể.
Do đó, các khuyến nghị sau đây được áp dụng:
- Việc sử dụng thuốc chống đông máu nên được quyết định riêng cho từng bệnh nhân.
- Khi điều trị bằng thuốc ức chế bổ sung, không cần thiết phải dùng thuốc chống đông máu phòng ngừa.
- Nếu đã bắt đầu điều trị bằng thuốc chống đông máu phòng ngừa trước khi điều trị bằng thuốc ức chế bổ sung, có thể xem xét ngừng điều trị sau khi hoạt động tan máu trở lại bình thường trong quá trình điều trị bằng thuốc ức chế bổ sung. Tuy nhiên, tuyệt đối không nên tự ý ngừng điều trị.
- Nếu đã xảy ra huyết khối, cần thực hiện chống đông máu. Thời gian điều trị phụ thuộc vào vị trí huyết khối và diễn biến của bệnh.
- Trong các tình huống rủi ro, ví dụ như nằm liệt giường, hạn chế vận động trong thời gian dài (bó bột), phẫu thuật hoặc đi xe buýt hoặc máy bay trong thời gian dài (> khoảng 4-6 giờ), nên thực hiện chống đông máu (ví dụ: bằng cách tiêm hoặc uống thuốc) để phòng ngừa, tùy thuộc vào giá trị tiểu cầu hiện tại.
- Nên phát hiện sớm các nhiễm trùng do vi khuẩn và điều trị triệt để bằng kháng sinh, vì nhiễm trùng có thể dẫn đến tình trạng PNH xấu đi nghiêm trọng kèm theo khủng hoảng tan máu.
- Trong trường hợp khủng hoảng tan máu/tan máu đột ngột, cần bổ sung đủ nước (hydrat hóa). Nếu cần, có thể phải điều trị bằng kháng sinh, truyền máu và bổ sung thuốc ức chế bổ sung, cũng như lọc máu (chạy thận) nếu chức năng thận suy giảm.
- Trong những trường hợp ngoại lệ, khi có suy giảm tủy xương (suy tủy xương) hoặc sau khi phát triển thiếu máu do thận (thận), việc sử dụng các yếu tố tăng trưởng tạo máu (huyết học), ví dụ như erythropoietin hoặc G-CSF, có thể là hữu ích.
- Nếu suy tủy xương (aplasia) là vấn đề chính so với PNH, có thể cần phải tiến hành liệu pháp ức chế miễn dịch hoặc cấy ghép tế bào gốc hoặc tủy xương, xem Thiếu máu bất sản, 5 Liệu pháp.
5.4 Chữa khỏi
Phương pháp điều trị PNH duy nhất có triển vọng chữa khỏi (phương pháp điều trị triệt để) là cấy ghép tủy xương hoặc tế bào gốc đồng loại. Tuy nhiên, phương pháp này đi kèm với tỷ lệ biến chứng (tỷ lệ mắc bệnh) và tử vong (tỷ lệ tử vong) đáng kể. Do đó, quyết định điều trị (chỉ định) cấy ghép phải được đưa ra một cách rất nghiêm ngặt, đặc biệt là kể từ khi có sẵn phương pháp điều trị bằng chất ức chế bổ sung.
Các lý do y tế để cấy ghép tế bào gốc là
- Các biến chứng huyết khối tái phát, đe dọa tính mạng, không đáp ứng với các phương pháp điều trị khác
- Thiếu máu tan máu rất nặng, không thể điều trị (kháng trị), cần phải truyền máu
- Sự hiện diện của một dòng PNH trong bệnh thiếu máu bất sản (AA) hoặc hội chứng rối loạn tạo máu (MDS), nếu bệnh thiếu máu bất sản hoặc hội chứng rối loạn tạo máu đã là lý do để cấy ghép
- Chuyển sang thiếu máu bất sản, nếu liệu pháp ức chế miễn dịch không được chỉ định, hoặc sang hội chứng rối loạn tạo máu
6 Tiên lượng
Do sự giảm đáng kể các sự kiện huyết khối dưới liệu pháp ức chế bổ sung, bệnh nhân được chẩn đoán PNH có tuổi thọ gần như tương đương với dân số bình thường.
7 Mong muốn có con/mang thai
Cho đến vài năm trước, bệnh nhân PNH thường được khuyên không nên mang thai do thường xuyên xảy ra các biến chứng đe dọa tính mạng của mẹ và con. Do liệu pháp kháng thể làm giảm đáng kể rủi ro này, vấn đề kế hoạch hóa gia đình lại trở nên quan trọng. Hiện tại, đã có các báo cáo về thai kỳ trong quá trình điều trị bằng Eculizumab, Ravulizumab và Crovalimab với kết quả rất đáng khích lệ, mặc dù số lượng trường hợp còn hạn chế. Các trường hợp mang thai này hầu như không có biến chứng và tất cả trẻ em đều khỏe mạnh. Tuy nhiên, nếu có mong muốn mang thai hoặc đang mang thai, bệnh nhân nên liên hệ với một trung tâm chuyên khoa về huyết học và phụ khoa để xác định hồ sơ rủi ro cá nhân của bệnh nhân và điều chỉnh liều lượng thuốc ức chế bổ sung nếu cần thiết.
8 Triển vọng
Hiện tại, các chất ức chế hệ thống bổ sung khác đang được thử nghiệm trong các nghiên cứu lâm sàng.
9 Đăng ký
Vì PNH là một bệnh rất hiếm gặp, thông tin liên quan đến bệnh và điều trị chỉ có thể thu được thông qua việc phân tích dữ liệu của càng nhiều bệnh nhân PNH càng tốt trên phạm vi quốc tế. Với mục đích này, Đăng ký bệnh nhân PNH quốc tế (PNH Registry) đã được thành lập và đóng cửa vào cuối năm 2024. Để tiếp tục hoạt động này, đặc biệt là với các phương pháp điều trị mới, một nhóm chuyên gia PNH quốc tế (International PNH Interest Group, IPIG) đã thành lập một sổ đăng ký mới. Kể từ năm 2025, sau khi có sự đồng ý của bệnh nhân, sổ đăng ký này sẽ ghi lại dữ liệu về diễn biến bệnh, điều trị và chất lượng cuộc sống dưới dạng ẩn danh 6 tháng một lần. Vì chỉ thông qua những thông tin như vậy mới có thể thu được những kiến thức mới về bệnh và cải thiện hơn nữa phương pháp điều trị, nên tất cả bệnh nhân PNH nên đồng ý cung cấp dữ liệu của mình cho sổ đăng ký.
HÃY THAM GIA!
Nếu quan tâm hoặc có thắc mắc, vui lòng gửi email đến Prof. Dr. med. Alexander Röth (alexander.roeth(at)ukessen.de) hoặc Prof. Dr. med. Hubert Schrezenmeier (h.schrezenmeier(at)blutspende.de).

