Thiếu máu bất sản (AA)
1 AA là gì?
2 Triệu chứng
3 Chẩn đoán
4 Diễn biến lâm sàng
5 Điều trị
6 Tiên lượng
7 Đăng ký
1 AA là gì?
1.1 Tổng quan
Thiếu máu bất sản là một bệnh huyết học không ác tính (không ác tính). Nguyên nhân của bệnh là do rối loạn chức năng tủy xương, dẫn đến giảm sản xuất tế bào máu.
Tùy thuộc vào nguyên nhân gây ra thiếu máu bất sản, người ta phân biệt giữa các dạng bẩm sinh (ví dụ: thiếu máu Diamond-Blackfan hoặc Fanconi, telomeropathy) và các dạng mắc phải. Cả hai dạng này đều có thể xuất hiện ở mọi lứa tuổi.
Rối loạn tạo máu sau hóa trị hoặc xạ trị không được gọi là thiếu máu bất sản.
1.2 Tỷ lệ mắc bệnh (dịch tễ học)
Tỷ lệ mắc bệnh (tỷ lệ mắc) ở Trung Âu là 2-3 ca mới trên 1 triệu người mỗi năm. Do đó, thiếu máu bất sản là một trong những bệnh rất hiếm gặp. Hầu hết những người mắc bệnh này ở độ tuổi từ 10 đến 25 tuổi và trên 60 tuổi, với tỷ lệ mắc bệnh ở cả hai giới là như nhau.
1.3 Nguyên nhân (bệnh sinh)
Theo các nghiên cứu, trong bệnh thiếu máu bất sản mắc phải, một phần của hệ thống miễn dịch tấn công các tế bào trong tủy xương. Đây là một loại tế bào lympho, ngăn chặn sự hình thành các tế bào máu mới thông qua quá trình tự miễn dịch này. Trong một số trường hợp thiếu máu bất sản mắc phải, người ta nghi ngờ nguyên nhân là do thuốc hoặc chất độc (khoảng 20%) hoặc nhiễm virus (khoảng 5%).
Tuy nhiên, trong hầu hết các trường hợp thiếu máu bất sản mắc phải (khoảng 75%), không thể xác định nguyên nhân gây ra bệnh, do đó nguồn gốc của bệnh vẫn chưa rõ ràng (vô căn). Tuy nhiên, cũng có những trường hợp mà một sự thay đổi bẩm sinh là nguyên nhân gây ra sự xuất hiện hoặc diễn biến của thiếu máu bất sản.
Các nghiên cứu gần đây cho thấy một phần đáng kể bệnh nhân bị thiếu máu bất sản mắc phải thực chất là mắc phải một dạng bẩm sinh, chỉ biểu hiện lâm sàng muộn. Hiện tại, tỷ lệ các trường hợp bẩm sinh chỉ được phát hiện ở tuổi trưởng thành là 5-15% trong tổng số các trường hợp thiếu máu bất sản ở người trưởng thành. Có thể giả định rằng tỷ lệ này sẽ tiếp tục tăng do các phương pháp chẩn đoán ngày càng cải tiến. Điều này rất quan trọng vì phương pháp điều trị cho nhóm bệnh nhân này khác với các trường hợp thiếu máu bất sản mắc phải. Điều này đặc biệt quan trọng đối với việc cấy ghép tế bào gốc.
1.4 Tiêu chí chẩn đoán và phân loại
Để có thể chẩn đoán bệnh thiếu máu bất sản, các tiêu chí sau phải được đáp ứng:
- Số lượng tế bào trong tủy xương (tế bào học) ít hơn 25% so với tủy xương khỏe mạnh, được đánh giá dựa trên sinh thiết tủy xương. Sản xuất tế bào có thể giảm (hypoplastic) hoặc hoàn toàn không có (aplastic) trong bệnh này.
- Giảm hai (bizytopenie) hoặc ba hàng tế bào (tri- hoặc panzytopenie) ở các mức độ khác nhau trong máu.
- Không có dấu hiệu hình thành (mới) mô liên kết trong tủy xương (xơ hóa) hoặc sự xâm lấn tủy xương bởi các tế bào ác tính (malign) hoặc các tế bào không thuộc tủy xương.
- Ngoài ra, không được có những thay đổi tế bào đáng kể (loạn sản) trong quá trình tạo máu (hematopoiesis).
- Gần đây không có xạ trị hoặc hóa trị nào có thể giải thích sự rối loạn chức năng tủy xương (suy tủy xương).
- Không có tiếp xúc với bức xạ phóng xạ.
Thiếu máu bất sản được phân loại dựa trên các chỉ số máu (xem bảng dưới đây) thành:
- không nặng Thiếu máu bất sản = nSAA (“non-severe AA”)/thiếu máu bất sản vừa phải (“Moderate AA”)
- Trầm trọng Thiếu máu bất sản = SAA („severe AA“)
- Rất trầm trọng Thiếu máu bất sản = vSAA („very severe AA“)
và có ý nghĩa quyết định đối với tiên lượng và điều trị.
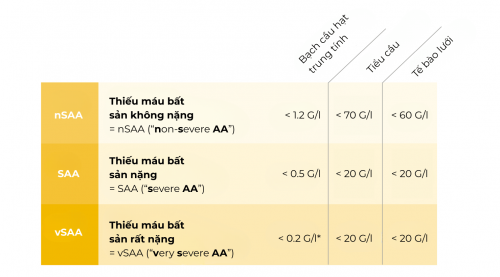
Phân loại thiếu máu bất sản dựa trên công thức máu (đếm tế bào và phết tế bào). Phải đáp ứng hai trong ba tiêu chí. *Để được phân loại là vSAA, tiêu chí bạch cầu hạt < 0,2 G/l phải được đáp ứng bắt buộc.
2 Triệu chứng
2.1 Thiếu máu
Sự giảm số lượng hồng cầu vận chuyển oxy (erythrocytes) có thể gây ra suy nhược, mệt mỏi và khó thở, thậm chí là tim đập nhanh, đặc biệt là khi gắng sức. Ngoài ra, bệnh nhân bị thiếu máu thường có biểu hiện da xanh xao, đặc biệt là lòng bàn tay, tuy nhiên, da xanh xao không phải là bằng chứng của thiếu máu.
2.2 Tăng khả năng nhiễm trùng</ span>
Sự giảm số lượng bạch cầu (leukocytes) làm cơ thể dễ bị nhiễm trùng hơn. Do hệ thống miễn dịch của cơ thể không hoạt động hiệu quả khi số lượng bạch cầu trung tính, một loại bạch cầu, giảm, nhiễm trùng có thể trở nên nguy hiểm đến tính mạng trong vòng vài giờ và dẫn đến nhiễm trùng máu.
Do đó, khi bị sốt, bạn cần thông báo ngay cho bác sĩ điều trị. Sốt được định nghĩa là nhiệt độ cơ thể trên 38 °C được đo hai lần trong vòng một giờ bằng nhiệt kế tai hoặc trên 38,3 °C được đo một lần bằng nhiệt kế tai.
2.3 Chảy máu
Khi số lượng tiểu cầu (thrombocytes) giảm, quá trình cầm máu có thể bị rối loạn. Khi đó, nướu răng sẽ chảy máu và xuất hiện các nốt ban xuất huyết, các vết chấm nhỏ trên da hoặc vết bầm tím (hematomas). Những hiện tượng này có thể xuất hiện một cách tự phát, tức là không có chấn thương trước đó. Khi quá trình cầm máu bị rối loạn, ngay cả một vết chảy máu hoặc chấn thương tương đối nhẹ (ví dụ như khi đi khám nha sĩ) cũng có thể trở nên nguy hiểm. Do đó, nếu bị chảy máu, bạn nên liên hệ ngay với bác sĩ điều trị để bác sĩ có thể quyết định xem có cần thực hiện các biện pháp đặc biệt (ví dụ như truyền tiểu cầu) hay không.
3 Chẩn đoán
Nếu có một hoặc nhiều triệu chứng và biểu hiện nêu trên, bác sĩ gia đình sẽ chỉ định xét nghiệm máu. Nếu phát hiện bất thường trong công thức máu, bệnh nhân sẽ được chuyển đến bác sĩ chuyên khoa về huyết học và ung thư.
Tại đó, một loạt các xét nghiệm khác sẽ được thực hiện:
- Tiền sử bệnh (tiền sử bệnh), bao gồm cả tiền sử gia đình, bao gồm ghi chép chi tiết các loại thuốc đã dùng
- Khám sức khỏe, ví dụ như các dấu hiệu thiếu máu và chảy máu
- Xét nghiệm tế bào
-
- Công thức máu vi thể khác biệt
- Tế bào lưới
- Chẩn đoán PNH (hemoglobin niệu kịch phát ban đêm) (một số lượng đáng kể tế bào PNH có thể được phát hiện trong tới 70% các trường hợp AA), xem PNH, 3 Chẩn đoán
-
- Hóa học lâm sàng
-
- Các thông số tan máu: đặc biệt là LDH, haptoglobin, bilirubin
- Đông máu: giá trị Quick, PTT, fibrinogen
- Tham số chức năng gan: AST, ALT và AP
- Tham số chức năng thận: Creatinine, axit uric
- Đường huyết
- Protein tổng, điện di, immunoglobulin
- Tham số viêm CRP
- Mức vitamin B12 và axit folic
- Tình trạng sắt: Ferritin. Nếu giá trị ferritin > 1000 ng/ml, cần kiểm tra thêm để xác định khả năng tổn thương cơ quan do quá tải sắt
- Chẩn đoán virus: Viêm gan A, B, C; HIV, EBV, CMV, Parvovirus B19
- Kháng thể kháng nhân và kháng DNA
-
- Chẩn đoán chức năng
-
- Siêu âm tim và vùng bụng trên (siêu âm)
- Chụp X-quang lồng ngực (thorax)
- Điện tâm đồ (EKG)
-
- Khám nghiệm đặc biệt
- Xác định kiểu gen HLA của bệnh nhân và anh chị em của bệnh nhân
- Xác định chiều dài telomere
- Nếu nghi ngờ mắc hội chứng suy tủy bẩm sinh, cần tiến hành chẩn đoán sâu hơn, ví dụ như phân tích gãy nhiễm sắc thể nếu nghi ngờ mắc bệnh thiếu máu Fanconi, xét nghiệm gen
Nếu xác nhận số lượng một hoặc nhiều dòng tế bào máu giảm mà không có nguyên nhân rõ ràng dẫn đến sự tiêu thụ hoặc phân hủy tăng cao của các tế bào máu này, thì cần tiến hành kiểm tra tủy xương ngay lập tức. Bằng cách này, có thể xác định xem có rối loạn tạo máu hay nguyên nhân khác hay không.
Để làm điều này, cần tiến hành chọc tủy xương, có thể thực hiện tại phòng khám ngoại trú. Dưới tác dụng của thuốc gây tê cục bộ (gây tê tại chỗ), bác sĩ sẽ dùng kim rỗng (kim Jamshidi) lấy một mẫu xương hình trụ (sinh thiết tủy xương, lấy mẫu tủy xương) từ xương chậu của bệnh nhân. Mẫu này có chiều dài khoảng 1,5 cm và đường kính 2-3 mm, sau đó được kiểm tra và đánh giá dưới kính hiển vi (mô học).
Ngoài ra, máu, tủy xương và các phần mỡ xương (“mảnh tủy”) cũng được lấy ra (chọc hút tủy xương), được phết lên kính hiển vi, sấy khô, nhuộm màu và cũng được đánh giá dưới kính hiển vi về tổng thể hoặc vị trí của chúng so với nhau (kiểm tra tế bào học).
Ngoài ra, các tế bào tủy xương có thể được kiểm tra di truyền, kết quả của việc kiểm tra này có thể giúp phân biệt với các bệnh khác.
Vì các bước thí nghiệm riêng lẻ trong quá trình sản xuất mô học tủy xương rất tốn thời gian, nên phải mất khoảng 1-2 tuần để có kết quả hoàn chỉnh. Nếu thấy sự giảm sút trong sự hình thành của hai hoặc ba hàng tế bào (hồng cầu, bạch cầu, tiểu cầu) theo tiêu chí chẩn đoán mà không có sự hiện diện đồng thời của các tế bào bị biến đổi bệnh lý (ví dụ: tế bào bạch cầu) và không có hóa trị hoặc xạ trị trước đó, thì người ta gọi đó là thiếu máu bất sản.
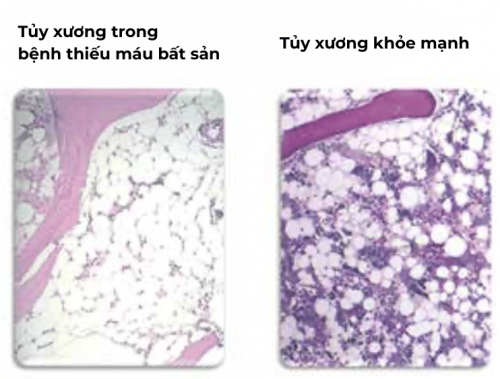
Kết quả kiểm tra tủy xương của một bệnh nhân bị thiếu máu bất sản so với tủy xương khỏe mạnh. Trong tủy xương bị bệnh, chủ yếu có thể nhận thấy mô liên kết và tế bào mỡ. Trong tủy xương khỏe mạnh, các tế bào máu nổi bật như những chấm nhỏ có màu khác nhau so với các tế bào mỡ trắng lớn.
Mục đích của các xét nghiệm này là
- loại trừ các bệnh khác,
- làm rõ các nguyên nhân có thể (căn nguyên),
- xác định mức độ nghiêm trọng của thiếu máu bất sản,
- xác định tiên lượng.
Đối với những bệnh nhân bị thiếu máu bất sản rất nặng và nặng, dưới 50 tuổi và có thể trạng tốt, nên tiến hành phân loại HLA cho bệnh nhân ngay khi chẩn đoán. Nếu có anh chị em ruột, họ cũng nên được phân loại để xác định khả năng hiến tặng tế bào gốc.
4 Diễn biến
Nếu không có liệu pháp điều trị cụ thể, thiếu máu bất sản ở người trưởng thành có thể gây tử vong trong 70% trường hợp.
Có khả năng bệnh thiếu máu bất sản chuyển sang hội chứng rối loạn tạo máu (MDS) hoặc bệnh bạch cầu tủy cấp tính (AML). Ngoài ra, một số bệnh nhân AA có đột biến đặc trưng của PNH, do đó các triệu chứng và nhu cầu điều trị của bệnh tiểu đêm paroxysmal (PNH) cũng có thể trở nên liên quan.
5 Điều trị
5.1 Tổng quan
Hồi phục tự phát về mặt huyết học (thuyên giảm tự phát) hầu như không xảy ra trong trường hợp suy tủy xương nặng.
Cần phải điều trị trong các trường hợp sau
- thiếu máu bất sản nặng (vSAA) và nặng (SAA)
- thiếu máu bất sản không nặng (nSAA) với sự giảm rõ rệt của ít nhất một dòng tế bào (cytopenia), dẫn đến nhu cầu truyền máu thường xuyên hoặc nguy cơ nhiễm trùng hoặc chảy máu
Trong khi vài thập kỷ trước, hầu như không có hy vọng chữa khỏi hoặc cải thiện lâu dài, thì ngày nay có nhiều khả năng đầy hứa hẹn. Có hai phương pháp điều trị chính: liệu pháp ức chế miễn dịch (IST) và cấy ghép tế bào gốc (SZT) hoặc cấy ghép tủy xương (KMT). Ngoài ra, còn có các liệu pháp đặc biệt cho một số nhóm bệnh nhân nhất định. Liệu pháp nào phù hợp với một bệnh nhân cụ thể phụ thuộc vào mức độ nghiêm trọng của bệnh, tuổi tác và các bệnh kèm theo có thể có của bệnh nhân, cũng như mức độ tương thích HLA (tương thích HLA) với một người hiến tủy xương có thể là người thân hoặc không phải người thân.
Nếu có chỉ định điều trị, cần bắt đầu điều trị càng sớm càng tốt để ngăn chặn sự tiến triển của bệnh và các biến chứng có thể xảy ra (ví dụ: thiếu máu nặng, nhiễm trùng, chảy máu và rối loạn đông máu). Do đó, việc lập kế hoạch điều trị sớm với sự hợp tác của một trung tâm chuyên khoa là rất quan trọng.
Quy trình điều trị cho bệnh nhân bị thiếu máu bất sản nặng và rất nặng được trình bày trong hình dưới đây.
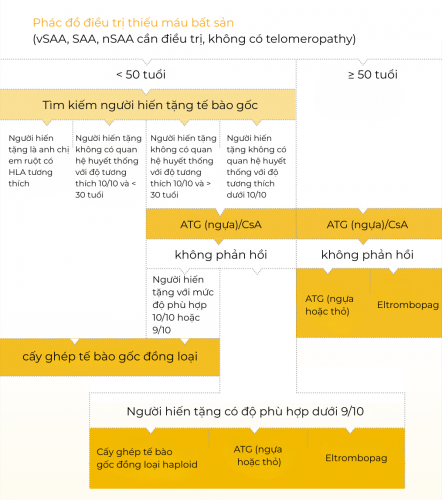
Biểu diễn đơn giản hóa rõ ràng của thuật toán điều trị. Thuật toán hoàn chỉnh được trình bày trong hướng dẫn của DGHO tại Onkopedia
5.2 Liệu pháp ức chế miễn dịch (IST)
Antithymozytenglobulin (ATG) và Ciclosporin (CsA)
Vì trong trường hợp thiếu máu bất sản mắc phải, hệ thống miễn dịch của cơ thể tấn công tủy xương của chính mình, nên thường chỉ định điều trị ức chế miễn dịch, đặc biệt là trong các trường hợp sau:
- Bệnh nhân vSAA hoặc SAA > 50 tuổi
- Bệnh nhân không có người hiến tặng HLA phù hợp (anh chị em ruột)
- Bệnh nhân vSAA hoặc SAA < 50 tuổi trong tình trạng thể chất kém
- Bệnh nhân nSAA/MAA có nguy cơ bị giảm tế bào máu nghiêm trọng trong ít nhất một dòng tế bào
Liệu pháp ức chế miễn dịch thường là sự kết hợp giữa thuốc antithymocyte globulin và ciclosporin. Điều này giúp tủy xương phục hồi. Trong quá trình điều trị, tình trạng máu thường xấu đi trong thời gian ngắn trước khi có sự cải thiện.
ATG là một kháng thể phá hủy các tế bào lympho T hoạt động quá mức và gây tổn thương tủy xương. Thông thường, ATG được tiêm vào một tĩnh mạch lớn qua một ống thông tĩnh mạch trung tâm (ZVK) trong 4-5 ngày. Trong quá trình điều trị bằng ATG, nếu cần, nên tăng hoặc duy trì số lượng tiểu cầu lên 30 G/l bằng cách truyền tiểu cầu, vì trong quá trình điều trị, số lượng tiểu cầu có thể giảm nhanh chóng. Để điều trị bằng ATG, bệnh nhân phải nhập viện khoảng 1-2 tuần. Tác dụng phụ của liệu pháp ATG có thể là các phản ứng dị ứng như phát ban và sốt. Để ức chế các tác dụng phụ cấp tính của ATG, một chế phẩm cortisone, ví dụ như prednisone hoặc prednisolone, cũng được tiêm trong một thời gian ngắn. Ngoài ra, còn có nguy cơ cao nhiễm một số tác nhân gây bệnh, do đó cần phải thực hiện các biện pháp phòng ngừa thích hợp.
Một yếu tố quan trọng khác ảnh hưởng đến hiệu quả điều trị bệnh là ciclosporin, một loại thuốc ức chế sự tiết ra các chất kích thích miễn dịch. Khi dùng CsA, cần tiến hành kiểm tra thường xuyên tại phòng thí nghiệm để điều chỉnh liều lượng nếu cần thiết nhằm đạt được hiệu quả tối ưu. Mục tiêu là đạt nồng độ thấp nhất trong máu từ 170–225 ng/ml. Để duy trì nồng độ ổn định, cần dùng thuốc rất đều đặn, cách nhau 12 giờ.
Các tác dụng phụ có thể xảy ra của liệu pháp CsA là nhiễm trùng, suy giảm chức năng thận, tăng huyết áp, tăng sinh nướu răng (tăng sản nướu răng), tăng trưởng tóc, co thắt cơ, rối loạn cảm giác hoặc run (rung giật). Các tác dụng phụ phụ thuộc vào liều lượng và thường biến mất khi ngừng liệu pháp CsA.
CsA được dùng dưới dạng viên nang hoặc nước uống trong ít nhất 12 tháng. Nếu đáp ứng điều trị rất tốt và ổn định, để tránh bệnh tái phát, khi ngừng điều trị, cần giảm liều CsA rất chậm và dần dần. Tuy nhiên, một số bệnh nhân phải dùng CsA lâu hơn hoặc vĩnh viễn để duy trì hiệu quả điều trị.
Nhờ liệu pháp ức chế miễn dịch tăng cường, khoảng 50-75% bệnh nhân có thể được chữa khỏi (thuyên giảm hoàn toàn, CR) hoặc ít nhất là cải thiện đáng kể (thuyên giảm một phần, PR), không cần truyền máu và giảm đáng kể nguy cơ nhiễm trùng và chảy máu. Phải mất khoảng 2-4 tháng, đối với một số bệnh nhân là 6 tháng, để các chỉ số máu được cải thiện. Mục tiêu là chấm dứt các triệu chứng lâm sàng và rủi ro. Để đạt được điều này, không cần thiết phải bình thường hóa hoàn toàn các chỉ số máu, điều thường không thể đạt được.
Nếu không có phản ứng, có thể xem xét lặp lại liệu pháp ức chế miễn dịch sau 4-6 tháng.
Trong trường hợp tái phát (tái phát), cũng có thể lặp lại liệu pháp ức chế miễn dịch, vì cơ hội đáp ứng lại là 30-60%.
Đi kèm với liệu pháp cụ thể, mỗi bệnh nhân nên được điều trị bằng liệu pháp hỗ trợ (supportive therapy) href=”#suppther”>liệu pháp hỗ trợ.
Alemtuzumab
Cũng có các loại thuốc khác hoạt động theo cơ chế ức chế miễn dịch tương tự. Trong số đó có Alemtuzumab, một kháng thể có tác dụng chống lại tế bào lympho T. Thuốc này được sử dụng trong điều trị bệnh bạch cầu lympho mãn tính (CLL) hoặc bệnh đa xơ cứng (MS), nhưng trong các nghiên cứu, thuốc này cũng cho thấy tỷ lệ đáp ứng tốt trong điều trị bệnh thiếu máu bất sản, đặc biệt là ở bệnh nhân cao tuổi. Một lợi thế của thuốc này là chỉ cần tiêm dưới da, do đó không cần phải nhập viện. Nếu bệnh nhân từng bị nhiễm virus cytomegalovirus (CMV), cần kiểm tra chỉ số máu này thường xuyên, vì nhiễm virus này có thể tái phát trong quá trình điều trị.
Các bệnh nhân không đáp ứng với các liệu pháp khác đã cho thấy tỷ lệ đáp ứng từ 37-48% khi sử dụng Alemtuzumab.
5.3 Cấy ghép đồng loại
Đối với bệnh nhân dưới 50 tuổi (điều quan trọng là tình trạng chung, “tuổi sinh học”) bị thiếu máu bất sản nặng hoặc rất nặng (SAA hoặc vSAA) và có anh chị em ruột là người hiến tặng hoàn toàn tương thích về cấu trúc tương thích mô (HLA) với bệnh nhân (HLA-ident), phương pháp điều trị ưu tiên (điều trị đầu tiên) là cấy ghép đồng loại.
Bệnh nhân dưới 30 tuổi cũng có thể nhận tế bào gốc từ người hiến tặng không có quan hệ huyết thống nhưng tương thích HLA (người hiến tặng ngoài gia đình) nếu họ không có người hiến tặng trong gia đình tương thích HLA. Điều quan trọng là phải tiến hành phân loại chi tiết (ít nhất 10 kháng nguyên HLA) và người hiến tặng và người nhận phải hoàn toàn tương thích.
Trong những năm gần đây, tỷ lệ biến chứng trong cấy ghép từ người hiến tặng không có quan hệ huyết thống có HLA tương thích đã giảm đáng kể. Do đó, cấy ghép từ người hiến tặng không có quan hệ huyết thống có HLA tương thích ngày càng được áp dụng nhiều hơn cho bệnh nhân dưới 50 tuổi và không đáp ứng với điều trị ức chế miễn dịch.
Mục tiêu của cấy ghép dị gen là thay thế tủy xương không hoạt động của bệnh nhân bằng tế bào gốc khỏe mạnh của người hiến tặng. Để làm được điều này, trước tiên tủy xương của bệnh nhân sẽ bị phá hủy bằng các biện pháp khác nhau (hóa trị, liệu pháp kháng thể, xạ trị). Quá trình điều trị này được thực hiện trong những ngày ngay trước khi cấy ghép.
Song song với đó, các tế bào gốc mới, khỏe mạnh sẽ được thu thập từ một người hiến tặng khỏe mạnh, có quan hệ huyết thống hoặc không có quan hệ huyết thống.
Các tế bào gốc có thể được lấy trực tiếp từ tủy xương bằng cách sinh thiết tủy xương dưới gây mê. Việc chọc vào xương chậu để lấy tủy xương có thể gây bầm tím và đau đớn trong vài ngày. Ngoài ra, còn có rủi ro chung của gây mê.
Ngoài ra, người hiến tặng sẽ được tiêm một loại thuốc kích thích sự hình thành bạch cầu hạt (G-CSF) trong vài ngày. Các tế bào gốc máu được sản sinh nhiều hơn do đó sẽ di chuyển từ tủy xương vào máu. Các tế bào gốc máu ngoại vi (PBSZ) này sau đó sẽ được lấy ra bằng một thiết bị đặc biệt, giống như khi hiến máu (Apherese). Quá trình này có thể gây ra các triệu chứng giống cúm và đau đớn.
Nếu tế bào gốc được lấy trực tiếp từ tủy xương, thì đó được gọi là cấy ghép tủy xương (KMT), còn nếu tế bào gốc được lấy bằng phương pháp Apherese, thì đó được gọi là cấy ghép tế bào gốc (SZT).
Các nghiên cứu cho thấy rằng điều trị thiếu máu bất sản bằng tế bào gốc từ máu ngoại vi có thể đi kèm với các biến chứng gia tăng, chẳng hạn như phản ứng thải ghép cấp tính hoặc mãn tính. Do đó, nếu có thể, nên sử dụng tế bào gốc được lấy trực tiếp từ tủy xương.
Bất kể tế bào gốc được thu thập bằng cách nào, chúng sẽ được làm sạch và kiểm tra các tác nhân gây nhiễm trùng. Sau đó, bệnh nhân sẽ nhận được tế bào gốc được hiến tặng. Quá trình cấy ghép diễn ra giống như truyền máu. Nếu mọi thứ diễn ra suôn sẻ, tế bào gốc của người hiến tặng sẽ “phát triển” và dẫn đến chức năng tủy xương và tạo máu bình thường. Để thực hiện cấy ghép, bệnh nhân phải nằm viện ít nhất 4 tuần.
Trong quá trình cấy ghép, bệnh nhân sẽ được dùng thuốc để phòng ngừa (phòng ngừa) nhiễm trùng do vi khuẩn và nấm. Ngoài ra, một loại thuốc cortisone, ví dụ như prednisolone, và ciclosporin (CsA) sẽ được dùng trong vài tháng để tác động lên hệ thống miễn dịch.
Các biến chứng có thể xảy ra do cấy ghép là:
- Tác dụng phụ độc hại trong quá trình điều trị chuẩn bị
- Nhiễm trùng
- Bệnh ghép chống chủ (GvHD)
- Từ chối ghép
Bệnh ghép chống chủ (GvHD): Trong trường hợp này, hệ thống miễn dịch được cấy ghép phản ứng lại với các tế bào của cơ thể. Điều này có thể xảy ra trong thời gian ngắn (cấp tính) hoặc muộn hơn và kéo dài (mãn tính), do đó trong một số trường hợp có thể cần phải ức chế hệ thống miễn dịch vĩnh viễn (liệu pháp ức chế miễn dịch).
5.4 Các lựa chọn điều trị khác
Danazol
Một số bệnh nhân bị thiếu máu bất sản có một rối loạn bẩm sinh hiếm gặp, trong đó các đầu của nhiễm sắc thể (telomere) bị ngắn lại, được gọi là telomeropathy. Sự ngắn lại của telomere dẫn đến rối loạn phân chia tế bào và do đó làm giảm sự hình thành các tế bào máu trong tủy xương.
Danazol, một biến thể tổng hợp của hormone sinh dục nam testosterone, đã được chứng minh là có thể làm dài telomere. Điều này có thể dẫn đến cải thiện các triệu chứng và thậm chí là bình thường hóa quá trình tạo máu.
Eltrombopag (Revolade®)
Kể từ năm 2015, Eltrombopag được chấp thuận sử dụng cho bệnh nhân người lớn bị thiếu máu bất sản nặng (SAA) khi họ
- không đáp ứng với liệu pháp ức chế miễn dịch trước đó hoặc
- đã được điều trị mạnh và
- không phù hợp để ghép tủy xương hoặc tế bào gốc.
Do tỷ lệ đáp ứng rất tốt trong các nghiên cứu lâm sàng, Eltrombopag đã được chấp thuận ở Hoa Kỳ để sử dụng kết hợp với hATG và CsA trong điều trị đầu tiên của bệnh thiếu máu bất sản. Thuốc này chưa được chấp thuận cho điều trị ban đầu ở EU. Tuy nhiên, do hiệu quả đã được chứng minh, Hiệp hội Huyết học và Ung thư Y học Đức khuyến nghị sử dụng Eltrombopag trong điều trị ban đầu SAA/vSAA mắc phải trong khuôn khổ các hướng dẫn của mình.
Eltrombopag có tác dụng điều chỉnh sự hình thành tế bào gốc máu và tiểu cầu. Thuốc này kích hoạt thrombopoietin, chất điều chỉnh sự hình thành tiểu cầu và máu (huyết tạo). Liều lượng hiệu quả đối với SAA là
150 mg/ngày. Nghiên cứu đã chứng minh rằng việc sử dụng Eltrombopag ở hầu hết bệnh nhân giúp cải thiện cả cũng như các giá trị hồng cầu và bạch cầu trung tính. Eltrombopag cũng giúp cải thiện hoặc bình thường hóa tế bào tủy xương. Ở những bệnh nhân trước đây cần truyền máu thường xuyên, số ngày đến lần truyền máu tiếp theo đã tăng lên hoặc họ không còn cần truyền máu nữa.
Khác
Các liệu pháp chưa được chứng minh hiệu quả, ví dụ như liệu pháp đơn trị bằng steroid hoặc liệu pháp đơn trị bằng các yếu tố tăng trưởng tạo máu, nên được tránh vì chúng chỉ làm mất thời gian và có thể làm tình trạng ban đầu của bệnh nhân xấu đi đáng kể so với các phương pháp điều trị đã được chứng minh hiệu quả.
5.5 Liệu pháp hỗ trợ (Supportive)
Phòng ngừa và điều trị nhiễm trùng, tránh chảy máu, chiến lược truyền máu phù hợp với từng cá nhân và điều trị quá tải sắt có ý nghĩa đặc biệt quan trọng trong điều trị hỗ trợ. Các biện pháp này đã được cải thiện trong những năm qua và góp phần cải thiện tỷ lệ sống sót, ngay cả khi điều trị không đạt được phản ứng hoàn toàn.
Nhiễm trùng
Trong trường hợp nhiễm trùng có sốt, cần đến gặp bác sĩ càng sớm càng tốt để chẩn đoán và bắt đầu điều trị.
Trong một số trường hợp, việc sử dụng kháng sinh để phòng ngừa vi khuẩn và thuốc chống nấm để phòng ngừa nấm có thể hữu ích.
- Ở bệnh nhân bị giảm bạch cầu hạt nặng (số lượng bạch cầu hạt/bạch cầu trung tính < 0,5 G/l)
- Đối với bệnh nhân đang điều trị bằng globulin kháng thymocyte (ATG) hoặc alemtuzumab, cần thực hiện các biện pháp phòng ngừa bổ sung chống lại các tác nhân gây bệnh khác (ví dụ: Pneumocystis jirovecii, cytomegalovirus).
Ngoài ra, khi số lượng bạch cầu hạt/bạch cầu trung tính giảm (< 0,5 G/l), cần tuân thủ các biện pháp phòng ngừa sau:
- Tránh tiếp xúc với những người bị nhiễm trùng
- Tránh tiếp xúc thân thể gần gũi với động vật
- Tránh những nơi đông người, đặc biệt là trong những tháng mùa đông
- Thực hiện các biện pháp vệ sinh thông thường, ví dụ như rửa tay, chăm sóc răng miệng, chú ý đến độ tươi và sạch sẽ của thực phẩm sống
- Tránh tiếp xúc gần gũi với bào tử nấm, đặc biệt là khi làm vườn, không làm sạch thùng rác sinh học hoặc đảo phân compost
Trong những trường hợp rất hiếm, ví dụ như nhiễm trùng nặng, có thể xem xét sử dụng các yếu tố tăng trưởng tạo máu G-CSF hoặc GM-CSF để kích thích hệ miễn dịch của cơ thể hoặc truyền máu tập trung bạch cầu (tập trung bạch cầu hạt).
Thông tin thêm có thể tìm thấy trong tài liệu “Nhiễm trùng? Không, cảm ơn!” của M. Exner và A. Simon thuộc Quỹ Hỗ trợ Bệnh nhân Bạch cầu & U lympho Đức.
Chảy máu
Do số lượng tiểu cầu giảm, bệnh nhân thiếu máu bất sản có thể bị chảy máu nghiêm trọng, thậm chí đe dọa tính mạng. Chảy máu có thể tăng lên hoặc kéo dài khi bị thương hoặc phẫu thuật, cũng như chảy máu đột ngột mà không có nguyên nhân rõ ràng.
Do đó, việc không hạn chế chức năng của các tiểu cầu hiện có bằng thuốc là rất quan trọng. Các loại thuốc như thuốc ức chế kết tập tiểu cầu là ví dụ điển hình, vì chúng ngăn chặn sự kết tập của tiểu cầu và do đó cản trở quá trình cầm máu.
Do đó, điều quan trọng là không được hạn chế chức năng của các tiểu cầu hiện có bằng thuốc. Các loại thuốc này bao gồm thuốc ức chế kết tập tiểu cầu, vì chúng ngăn chặn sự kết tập của tiểu cầu và do đó cản trở quá trình cầm máu. Vì vậy, việc sử dụng thuốc ức chế kết tập tiểu cầu như axit acetylsalicylic (ASS) cần được đánh giá một cách cực kỳ thận trọng, đặc biệt là khi số lượng tiểu cầu rất thấp, và cần được cân nhắc kỹ lưỡng.
Đối với phụ nữ có kinh nguyệt ra nhiều, để tránh mất máu quá nhiều khi thiếu tiểu cầu, có thể tạm thời ngừng kinh nguyệt bằng liệu pháp hormone, ví dụ như uống thuốc tránh thai liên tục hoặc tiêm thuốc 3 tháng một lần.
Phương pháp chính để tránh chảy máu và điều trị chảy máu hiện có là truyền huyết tương tiểu cầu.
Truyền máu (truyền huyết tương)
Truyền máu là cần thiết đối với nhiều bệnh nhân để đảm bảo sức khỏe thể chất và chất lượng cuộc sống cũng như để tránh các biến chứng chảy máu. Truyền máu có thể tạm thời thay thế các tế bào máu bị thiếu khi có các triệu chứng tương ứng (thiếu máu, chảy máu). Trong quá trình này, không phải toàn bộ máu được truyền (truyền máu), mà chỉ truyền loại tế bào cần thiết (hồng cầu hoặc tiểu cầu).
Để sản xuất huyết tương, sau khi hiến máu, máu sẽ được kiểm tra để loại trừ các bệnh truyền nhiễm, sau đó các tế bào bạch cầu sẽ được loại bỏ, và cuối cùng các thành phần máu khác nhau sẽ được tách ra và cô đặc. Các thành viên trong gia đình không được phép hiến máu, vì việc hiến máu có mục đích cụ thể này tiềm ẩn những rủi ro đặc biệt.
Truyền hồng cầu/huyết tương hồng cầu (truyền EK)
Để đảm bảo khả năng tương thích tốt, chế phẩm được sử dụng không chỉ được lựa chọn theo nhóm máu (A, B, AB, 0) và yếu tố Rhesus, mà mỗi chế phẩm riêng lẻ còn được kiểm tra riêng cho từng bệnh nhân. Để làm được điều này, trong một thử nghiệm tương thích, được gọi là thử nghiệm chéo, máu của bệnh nhân được trộn với máu từ hồng cầu cô đặc (EK) và được kiểm tra. Đặc biệt khi có kháng thể, việc tìm kiếm hồng cầu cô đặc phù hợp có thể mất nhiều thời gian hơn. Nếu bệnh nhân âm tính với virus cytomegalovirus (CMV) và có khả năng cấy ghép tủy xương hoặc tế bào gốc sau này, nên sử dụng hồng cầu cô đặc âm tính với CMV.
Nói chung, nên sử dụng hồng cầu cô đặc một cách thận trọng, vì chúng có thể dẫn đến quá tải sắt trong cơ thể. Các chỉ định cho truyền máu là
- suy giảm sức khỏe rõ rệt kèm theo mệt mỏi hoặc khó thở, ví dụ như khi gắng sức, và tùy thuộc vào các bệnh kèm theo, ví dụ như suy tim
- hàm lượng hemoglobin rất thấp (< 8 g/dl)
Nói chung, đối với liệu pháp truyền máu:
Càng nhiều càng tốt, càng ít càng tốt!
Do đó, chỉ định truyền máu phải được cân nhắc riêng cho từng bệnh nhân dựa trên các yếu tố sau:
- triệu chứng lâm sàng (ví dụ: nhịp tim, nhịp thở, khó thở, dấu hiệu chảy máu, sốt, nhiễm trùng…)
- triệu chứng chủ quan (ví dụ: suy giảm sức khỏe rõ rệt, mệt mỏi, suy nhược, đau đầu, ù tai
…) - các bệnh kèm theo/tiền sử cá nhân (ví dụ: suy tim, chảy máu)
- Thuốc/phương pháp điều trị (ví dụ: liệu pháp ATG, phẫu thuật)
- Khả năng theo dõi và truyền máu ngắn hạn (ngoại trú/nội trú)
Chiến lược truyền máu thận trọng áp dụng chủ yếu cho những bệnh nhân có kế hoạch cấy ghép tế bào gốc đồng loại. Trong trường hợp cấy ghép tế bào gốc được lên kế hoạch, tuyệt đối không được truyền máu từ người thân.
Truyền tiểu cầu/huyết tương tiểu cầu (truyền TK)
Trong trường hợp chảy máu, có thể truyền huyết tương (huyết tương, TK) để tránh các biến chứng. Vì chảy máu khi số lượng tiểu cầu thấp có thể là tình trạng cấp cứu đe dọa tính mạng, nên trong những trường hợp này phải hành động ngay lập tức. Nếu số lượng tiểu cầu rất thấp, huyết tương cũng có thể được truyền để phòng ngừa. Tuổi thọ của tiểu cầu chỉ vài ngày. Do đó, nếu sản xuất tiểu cầu trong tủy xương rất ít hoặc không có, có thể cần phải truyền tiểu cầu cô đặc nhiều lần trong tuần.
Tiểu cầu mang các đặc điểm mô (dấu hiệu HLA) khác nhau ở mỗi người. Một số bệnh nhân có kháng thể chống lại các dấu hiệu HLA này. Điều này có thể xảy ra một cách tự phát, trong bối cảnh bệnh tật hoặc sau khi mang thai. Nếu có các kháng thể HLA như vậy, các tiểu cầu được truyền sẽ bị phá hủy ngay lập tức, dẫn đến sự gia tăng tiểu cầu không đủ sau khi truyền huyết tương tiểu cầu. Đối với những bệnh nhân này, huyết tương tiểu cầu tương thích HLA đặc biệt phải được sản xuất từ những người hiến tặng có đặc điểm HLA phù hợp.
Chỉ định truyền huyết tương tiểu cầu là:
- khi số lượng tiểu cầu < 20 G/l và sốt > 38° C, nhiễm trùng, có dấu hiệu chảy máu hoặc có tiền sử chảy máu nặng (WHO cấp 3 hoặc 4) cũng như khi có hiện tượng miễn dịch dị ứng (kháng thể HLA, xem ở trên)
- nếu không có rủi ro làm tăng nguy cơ chảy máu (ví dụ: sốt, nhiễm trùng, tiền sử chảy máu nặng, miễn dịch dị ứng), thì chỉ cần truyền máu khi số lượng tiểu cầu < 5 G/l. Điều kiện tiên quyết là phải kiểm tra thường xuyên và chặt chẽ (ví dụ: ít nhất một lần mỗi tuần), không có dấu hiệu chảy máu (ví dụ: ban xuất huyết) và có thể truyền máu nhanh chóng khi có dấu hiệu chảy máu.
- “Giới hạn riêng cho từng bệnh nhân”: Nhiều bệnh nhân có giới hạn ổn định, khi giảm xuống dưới giới hạn này sẽ xuất hiện các dấu hiệu chảy máu mạnh hơn.
- Trước và trong quá trình điều trị ATG, giá trị tiểu cầu nên được nâng lên 50 G/l, vì truyền ATG có thể dẫn đến giảm tiểu cầu nhanh chóng.
- Trước khi phẫu thuật hoặc can thiệp, bác sĩ điều trị phải được thông báo trước về bệnh thiếu máu bất sản và tốt nhất là được cung cấp kết quả xét nghiệm máu mới nhất!
Quá tải sắt
Với mỗi hồng cầu cô đặc, lượng sắt được hấp thụ gấp hơn 100 lần lượng sắt được cung cấp hàng ngày qua thức ăn. Do cơ thể con người không thể bài tiết sắt một cách chủ động, sắt sẽ được tích trữ trong các cơ quan khác nhau, chủ yếu là gan, tim, thận, tủy xương (xem bảng 2) và có thể gây tổn thương cho các cơ quan này. Bệnh nhân bị thiếu máu bất sản hoặc hội chứng rối loạn tạo máu (MDS) có nguy cơ bị quá tải sắt ngay cả khi không được truyền máu, vì chức năng tủy xương kém làm giảm sự hình thành hồng cầu mới và sắt không thể được sử dụng hoàn toàn để tạo ra các tế bào hồng cầu mới.
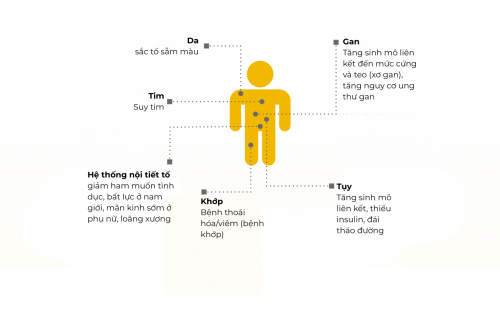
Các biến chứng của quá tải sắt
Thông thường, trong những tháng đầu tiên sau khi chẩn đoán, nồng độ sắt dự trữ (ferritin) hoặc sắt trong gan chưa đạt đến mức cần điều trị ngay lập tức để liên kết và loại bỏ sắt dư thừa (điều trị bằng chelat). Do đó, nên chờ ít nhất 6 tháng sau khi bắt đầu điều trị ức chế miễn dịch. Trong trường hợp cần truyền máu thường xuyên, liệu pháp chelat được chỉ định khi nồng độ ferritin huyết thanh trên 1.000 µg/l. Điều này đặc biệt áp dụng cho các bệnh nhân cần ghép tạng, vì quá tải sắt đi kèm với tỷ lệ tử vong liên quan đến ghép tạng cao hơn và tỷ lệ mắc bệnh cao hơn.
Các loại thuốc hiện nay được sử dụng để điều trị quá tải sắt thường được dung nạp tốt. Các tác dụng phụ chính bao gồm buồn nôn, tiêu chảy và rối loạn chức năng thận, nhưng các triệu chứng này sẽ giảm dần sau khi ngừng dùng thuốc.
Nếu ferritin huyết thanh dưới 1.000 µg/l, có thể xem xét ngừng điều trị trong trường hợp quá tải sắt do truyền máu, tùy thuộc vào nhu cầu truyền máu của từng cá nhân. Tuy nhiên, điều này phải luôn được thực hiện sau khi tham khảo ý kiến của bác sĩ điều trị.
Nếu không cần truyền máu và nồng độ hemoglobin đủ cao, liệu pháp lấy máu (lượng máu lấy tùy theo từng trường hợp, ví dụ: lượng máu lấy ít như 100 ml mỗi lần) được khuyến nghị như một phương pháp điều trị hiệu quả và ít tác dụng phụ đối với tình trạng quá tải sắt.
Nói chung, tình trạng quá tải sắt cần được kiểm tra thường xuyên và điều trị cần được điều chỉnh.
Thông tin thêm có thể tìm thấy trong tài liệu “Quá tải sắt do truyền máu” của Quỹ Hỗ trợ Bệnh nhân Bạch cầu & U lympho Đức.
Hoạt động
Đối với bệnh nhân bị thiếu máu bất sản, hoạt động thể chất và vận động là hữu ích tùy thuộc vào chỉ số máu và tình trạng sức khỏe. Tuy nhiên, cần chú ý để không bị quá sức. Do đó, nên tập thể dục trong khi kiểm soát nhịp tim. Điều này đặc biệt quan trọng đối với bệnh nhân thiếu máu, vì khi số lượng hồng cầu giảm, cơ thể thường cố gắng bù đắp sự thiếu hụt này bằng cách tăng nhịp tim, điều này có thể dẫn đến quá tải cho tim. Đối với bệnh nhân giảm tiểu cầu, cần tuyệt đối tránh các môn thể thao có nguy cơ chấn thương, ví dụ như võ thuật hoặc leo núi.
Phục hồi chức năng
Nếu bệnh thiếu máu bất sản khiến bệnh nhân không thể tham gia vào cuộc sống “bình thường” như trước đây, các biện pháp phục hồi chức năng, vật lý trị liệu ngoại trú hoặc chăm sóc tâm lý hoặc tâm lý trị liệu có thể hữu ích. Các biện pháp này nên được điều chỉnh riêng cho từng bệnh nhân.
Nếu có kế hoạch điều trị chuyên sâu, thì chỉ nên thực hiện các biện pháp phục hồi chức năng sau khi kết thúc điều trị. Vật lý trị liệu hoặc trị liệu tâm lý hoặc tâm lý trị liệu cũng hữu ích trong quá trình điều trị.
Khi tái hòa nhập một đứa trẻ bị thiếu máu bất sản sau khi kết thúc liệu pháp ức chế miễn dịch hoặc cấy ghép, do áp lực tâm lý xã hội lớn đối với gia đình, các biện pháp hướng đến gia đình tại một cơ sở chăm sóc sau ung thư nhi khoa có thể là hữu ích.
6 Tiên lượng
Số lượng bạch cầu hạt càng cao và tuổi của bệnh nhân tại thời điểm chẩn đoán càng nhỏ, tiên lượng càng tốt.
Dữ liệu về tỷ lệ sống sót sau các liệu pháp điều trị khác nhau được nêu dưới đây là dữ liệu thống kê. Điều này có nghĩa là dữ liệu này không thể tự động áp dụng cho từng bệnh nhân. Danh sách này chỉ nhằm cung cấp một cái nhìn tổng quan về những cải thiện trong khả năng điều trị và tỷ lệ sống sót trong những năm gần đây. Thường có những nhóm nhỏ không được tính đến ở đây. Đối với tất cả các hình thức điều trị cụ thể, kết quả đối với bệnh nhân dưới 20 tuổi rõ ràng tốt hơn so với bệnh nhân trên 20 tuổi. Điều tương tự cũng áp dụng cho bệnh nhân dưới 40/50 tuổi so với bệnh nhân trên 40/50 tuổi. Đối với cấy ghép tế bào gốc, kết quả tốt hơn đáng kể nếu người hiến tặng cung cấp tế bào gốc trực tiếp từ tủy xương chứ không phải tế bào gốc ngoại vi lấy từ máu.
Theo dữ liệu được công bố, tỷ lệ sống sót tổng thể đối với SAA/vSAA sau 3-6 năm và được phân chia theo các hình thức điều trị cụ thể khác nhau:
- sau SZT đồng loại từ người hiến tặng trong gia đình HLA-identem 75–90 %
- sau SZT đồng loại từ người hiến tặng không có quan hệ huyết thống HLA-identen 65–73 %
- sau điều trị ATG/CsA 76–96 %
7 Đăng ký
Bệnh nhân có bằng chứng về một dòng PNH có thể được ghi vào sổ đăng ký PNH quốc tế (PNH Registry) qua Bệnh viện Đại học Essen để có thể thu thập thêm thông tin về nhóm bệnh nhân AA này.
Nếu quan tâm hoặc có thắc mắc, vui lòng gửi email đến Prof. Dr. med. Alexander Röth (alexander.roeth(at)uk-essen.de).
Bệnh nhân mắc telomeropathy có thể được ghi vào Đăng ký AA-BMF tại Bệnh viện Đại học Aachen để có thể thu thập thêm thông tin về nhóm bệnh nhân AA này.
Nếu quan tâm hoặc có thắc mắc, vui lòng gửi email đến Prof. Dr. med. Tim H. Brümmendorf (tbruemmendorf(at)ukaachen.de).

